Chương Sự năng lượng điện li là chương khai mạc của lịch trình Hoá học tập lớp 11, chính vì vậy việc ôn tập luyện và reviews năng lượng trải qua Đề đánh giá 1 tiết hoá 11 chương 1 đem đáp án là vô nằm trong quan trọng, nó vừa vặn tập luyện kĩ năng, vừa vặn gia tăng kỹ năng và kiến thức vẫn học tập. Chương Sự năng lượng điện li cung ứng lý thuyết chủ yếu, xuyên thấu mang lại học tập kì 1 lớp 11 và là nền tảng mang lại năm học tập lớp 12. Bạn đang xem: đề kiểm tra 1 tiết hóa 11 chương 1 tự luận
Dưới đấy là Đề đánh giá 1 tiết hoá 11 chương 1 đem đáp án cụ thể bao hàm cả trắc nghiệm và tự động luận nhằm những em đơn giản dễ dàng tìm hiểu thêm.


Đề đánh giá 1 tiết hoá 11 chương 1 đem đáp án trang 1

Đề đánh giá 1 tiết hoá 11 chương 1 đem đáp án trang 2
II. Đề đánh giá 1 tiết hoá 11 chương 1 : PHẦN ĐÁP ÁN
Dưới đấy là tiếng giải cụ thể mang lại Đề đánh giá 1 tiết hoá 11 chương 1 đem đáp án
1. TRẮC NGHIỆM
Câu 1: Dung dịch đem tính axit càng mạnh thì pH càng nhỏ (pH < 7), tính bazơ càng mạnh thì pH càng rộng lớn (pH > 7).
NaOH: bazơ mạnh
NH3: bazơ yếu
NaCl: muối hạt (pH=7)
H2SO4: axit mạnh
Sắp xếp bám theo pH tăng dần: H2SO4 < NaCl < NH3 < NaOH
Chọn C.
Câu 2: Phương trình ion thu gọn:
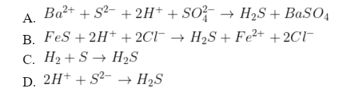
Chọn D.
* Lưu ý: - Các hóa học phân li trọn vẹn đi ra ion: axit mạnh, bazơ mạnh, đa số muối hạt tan.
- Các hóa học ghi bên dưới dạng phân tử: hóa học năng lượng điện li yếu đuối, kết tủa, khí.
Câu 3: Định luật bảo toàn năng lượng điện tích: 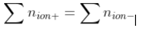
Vậy biểu thức chính là: 3a + 2b = c +2d
Chọn C.
Câu 4:
A. FeCl3, H2SO4 năng lượng điện li mạnh; CaCO3 là kết tủa
B. Na2SO4, CH3COONa năng lượng điện li mạnh; Fe(OH)3 là kết tủa
C. HCl, CH3COONH4, NaCl năng lượng điện li mạnh
D. NaOH, Fe2(SO4)3 năng lượng điện li mạnh; CH3COOH năng lượng điện li yếu
Chọn C.
Lưu ý: Các hóa học năng lượng điện li mạnh là những axit mạnh, bazơ mạnh, đa số những muối hạt tan.
Câu 5: Dung dịch bazơ tiếp tục thực hiện mang lại phenolphtalein hoá hồng.
Chọn A.
Câu 6: Theo thuyết A-re-ni-ut hóa học lưỡng tính là hóa học Khi tan nội địa vừa vặn phân li đi ra ion H+ vừa vặn phân li đi ra ion OH-.
A. Fe(OH)2 là hóa học kết tủa nên ko phân li.
B, C đều là bazơ mạnh.
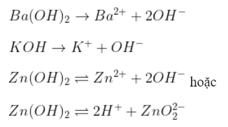
Chọn D.
Câu 7:
H2S, HClO là hóa học năng lượng điện li yếu đuối, phân li ko trọn vẹn nên dùng mũi thương hiệu 2 chiều.
KOH, NaCl là hóa học năng lượng điện li mạnh, phân li trọn vẹn trở nên ion, dùng mũi thương hiệu một chiều.
Chọn B.
Câu 8:
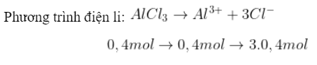
Chọn C.
Câu 9: pOH = -log[OH-]= -log(0,0001) = 4 → pH = 14-4=10
Chọn A.
Xem thêm: Xem bóng đá miễn phí trên Cakhia TV - Website hàng đầu Việt Nam
Câu 10: PTHH:
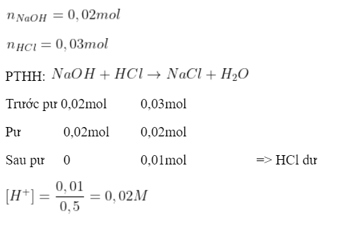
Chọn A.
Câu 11: HF là axit yếu đuối nên là hóa học năng lượng điện li yếu đuối.
Chọn C.
Câu 12: NaCl khan ở hiện trạng rắn nên ko dẫn được năng lượng điện.
Chọn D.
Câu 13: Muối axit là muối hạt tuy nhiên hiđro nhập gốc axit vẫn tồn tại năng lực phân li đi ra ion H+.
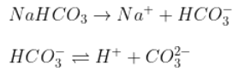
Vậy NaHCO3 là muối hạt axit.
Chọn D.
Câu 14: Điều khiếu nại nhằm xẩy ra phản xạ trao thay đổi nhập hỗn hợp là thành phầm cần đem kết tủa, hoặc hóa học khí hoặc hóa học năng lượng điện li yếu đuối.
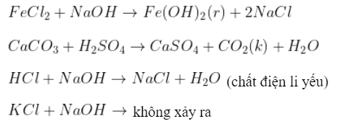
Chọn C.
Câu 15: Ca(OH)2 là bazơ mạnh, NaHCO3, Al2(SO4)3 là muối hạt tan, nên đều là hóa học năng lượng điện li mạnh nên lúc viết lách phương trình năng lượng điện li dùng mũi thương hiệu một chiều.
H3PO4 là axit yếu đuối, là hóa học năng lượng điện li yếu đuối nên lúc viết lách phương trình năng lượng điện li dùng mũi thương hiệu hai phía.
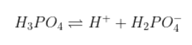
Chọn C.
Câu 16: Phản ứng trao thay đổi ion nhập hỗn hợp những hóa học điện li xẩy ra Khi thành phầm tạo trở nên đem hóa học kết tủa hoặc hóa học cất cánh khá hoặc hóa học điện li yếu đuối.
Chọn A.
Câu 17:
pH < 7 môi trường thiên nhiên axit, thực hiện quỳ tím hoá đỏ gay.
pH = 7 môi trường thiên nhiên tủng tính, ko thay đổi color quỳ tím.
pH > 7 môi trường thiên nhiên bazơ, thực hiện quỳ tím hoá xanh lơ.
pH càng nhỏ thì tính axit càng mạnh, chính vì vậy pH tăng, tính axit hạn chế.
Chọn B.
Câu 18: Các ion nằm trong tồn tại nhập một hỗn hợp, tức thị thân thích bọn chúng ko xẩy ra phản xạ này.
Các ion không cùng tồn tại nhập một hỗn hợp, tức thị thân thích bọn chúng đem xẩy ra phản xạ tạo ra trở nên kết tủa, hóa học khí hoặc hóa học năng lượng điện li yếu đuối.
Xét câu c,

Các câu a, b, d những ion này kết phù hợp với nhau đều tạo ra trở nên muối hạt tan nên vẫn tồn bên trên nhập và một hỗn hợp.
Chọn C.
Câu 19: H+ + OH- → H2O
Phản ứng này xẩy ra chính vì H2O là hóa học năng lượng điện li yếu đuối.
Chọn B.
Lưu ý: Xem lại ĐK nhằm xẩy ra phản xạ trao thay đổi ion nhập hỗn hợp hóa học năng lượng điện li.
Câu 20: [OH-]=2.10-3 => pOH = - log(2.10-3) = 2,7.
=> pH = 14-2,7 = 11,3
pH > 7 là môi trường thiên nhiên kiềm.
Chọn D.
2. TỰ LUẬN
Câu 1:
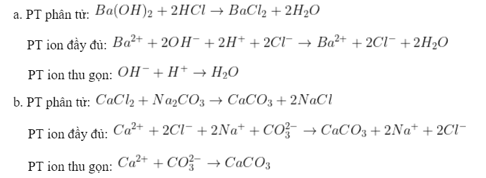
Câu 2:

Xem thêm: doraemon và nobita
Câu 3:

Với những thắc mắc và tiếng giải cụ thể của Đề Kiểm Tra 1 Tiết Hoá 11 Chương 1 Có Đáp Án trên phía trên, những em vừa vặn hoàn toàn có thể thực hiện bài bác đánh giá vừa vặn hoàn toàn có thể ôn tập luyện lại nội dung kỹ năng và kiến thức vẫn học tập của chương Sự năng lượng điện li. Từ ê, nắm rõ lí thuyết và áp dụng nhập bài bác tập luyện, đáp ứng cho những bài bác đánh giá bên trên lớp. Chúc những em triển khai xong bài bác tốt!











Bình luận